Как подобрать ключ к машине иммунитета

С каждым годом средняя продолжительность жизни населения Земли растет. Но, несмотря на положительную динамику, забота ученых и врачей о здоровье людей не останавливается ни на минуту. Каждый год в мире умирает несколько десятков миллионов людей. Причем 18% смертельных случаев приходится на инфекционные заболевания. Надо признать огромный прогресс человечества в улучшении ситуации, ведь всего 30 лет назад этот показатель составлял 35%. Несмотря на это, «гонка вооружений» с микробами не заканчивается никогда. В 2019 году бактерии, невосприимчивые к антибиотикам, напрямую вызвали смерть более миллиона людей, а также негативно повлияли на исход более 5 миллионов случаев заболеваний.
Изобретение новых методов воздействия на иммунный ответ является одной из важнейших задач здравоохранения. И здесь одним из наиболее перспективных направлений является модификация уже существующих иммунных систем организма.
Для того, чтобы усилить иммунный ответ, можно воспользоваться рядом подходов. Одним из них является введение в организм антимикробных пептидов (АМП). Они не только способны встраиваться в мембраны бактерий и вызывать их разрушение (лизис), но и повышать эффективность механизмов приобретенного иммунитета. К сожалению, разработка подобных пептидов ‒ очень затратная задача, которая часто заканчивается ничем. В клинических исследованиях часто подтверждается не только эффективность получаемых АМП, но и их высокая токсичность. Схожими особенностями обладают и антитела, которые ученые также пытаются использовать для борьбы с болезнетворными микроорганизмами.
Другим подходом, который применяют на практике, является воздействие на Толл-подобные рецепторы (TRL). Эти рецепторы имеют важную роль в распознании чужеродных патогенов. На данный момент у человека идентифицировано 10 типов TRL. Активация этих рецепторов с помощью химических веществ, например, флагеллина, помогает защищать людей от пневмонийных инфекций или даже проказы.
Противовоспалительные молекулы цитокинов могут как сами изменять иммунный ответ, так и усиливать воздействие других лекарств. Однако взаимодействие цитокинов с живым организмом очень сложно, неспецифично и сфокусировано в основном на активации врожденного, а не приобретенного иммунитета.
Одним из наиболее эффективных методов помощи организму является воздействие на молекулы комплекса гистосовместимости (MHC). Эти сложные белки встроены в мембрану всех наших клеток и отвечают за взаимодействия разных иммунных систем с целью презентации фрагментов патогенов на их поверхности. Некоторые бактерии (например, туберкулёзная палочка и сальмонелла) специально пытаются подавлять эту систему защиты, а при онкологических заболеваниях уровень экспрессии MHC снижается.
Активация системы MHC возможна следующими терапевтическими методами.
При лечении онкологических заболеваний используется препарат Биринапант, представляющий собой миметик SMAC (Second mitochondria-derived activator of caspase). За счет активации SMAC препарат стимулирует экспрессию MHC и за счет этого повышает чувствительность опухолевых клеток к действию цитотоксических Т-лимфоцитов.
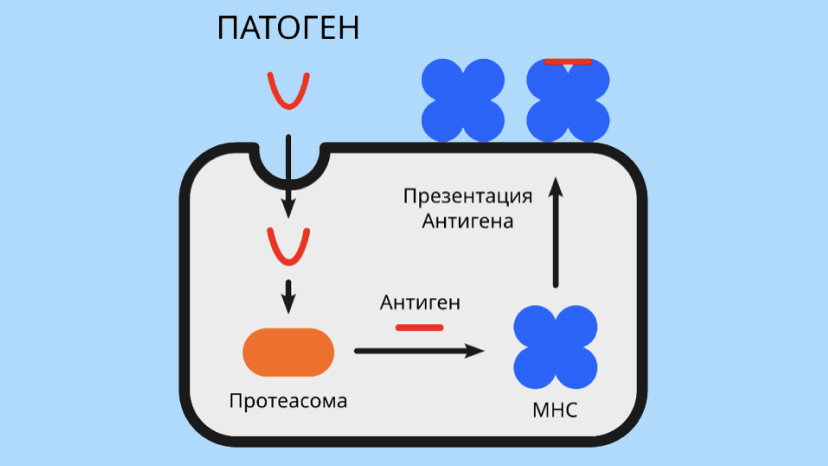
Другим подходом к активации MHC является введение в организм участков определенных антигенов. Во многом это напоминает вакцинацию. К препаратам, в которых используется данный подход, относятся синтетические пептиды, встраивающиеся в молекулы MHC, и, таким образом, презентирующие себя клеткам иммунной системы. Вводить такую «вакцину» пациенту необходимо в процессе болезни. Проблема использования синтетических пептидов-антигенов состоит в том, что для успешного лечения нужно точно знать, какой микроорганизм вызывает инфекцию.
В качестве лекарственных средств, повышающих уровень экспрессии молекул MHC, и тем самым, усиливающих антиген презентацию, могут также выступать препараты человеческого интерферона-гамма. Например, американский препарат Actimune используется для лечения хронической гранулематозной болезни.
Также можно воздействовать на молекулы MHC с помощью антител, которые, связываясь с комплексом гистосовместимости, могут менять его форму (конформацию), тем самым изменяя иммунный ответ. Однако данный подход несет в себе недостатки, связанные с терапевтическим использованием антител (в первую очередь речь здесь идет о высокой стоимости терапии и побочных эффектах). Одним из способов преодоления указанных недостатков является технологическая обработка антител. Примером лекарства, для получения которого используется данная технология, является российский противовирусный препарат Рафамин. Технологически обработанные антитела, входящие в его состав, инициируют конформационные изменения белков гистосовместимости с целью мягкого изменения их иммунной активности с минимальными побочными эффектами.
Человеческий иммунитет – чрезвычайно сложная система. За последние десятилетия научное понимание запутанных каскадов иммунных реакций, постоянно происходящих в нашем организме, значительно углубилось. Уже сегодня ученые могут использовать знания, полученные в данной области, для создания новых эффективных лекарств.